| 可见分光光度法测定杜仲叶中的绿原酸 |
| 发布时间:2010-10-20 信息来源:admin 发布人:admin 点击次数:4093 |
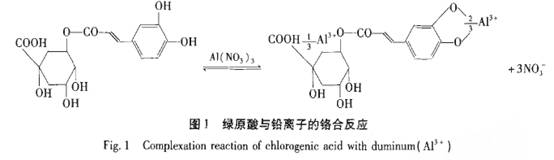
袁华,邓良,孙炎彬,杨小俊,闫志国,吴元欣+ (武汉工程大学化工与制药学院,武汉430073) 摘要:研究杜仲叶中绿原酸含量的检测方法。利用绿原酸和铝离子的络合显色反应,采用可见分光光度法在波长530 nm处测定杜仲叶中绿原酸量。绿原酸质量浓度在1.7×10-4~一1.O×10-2~g・L-1。1之间线性关系良好,线性相关系数为0.9995。秋、夏叶中加标回收率分别为98.0%,101.0%。该方法简便、实用、准确。 关键词:杜仲叶;绿原酸;可见分光光度法 杜仲(Eucommia Ulmoides 0liv.)是我国特有的经济树种,其药用价值历来受到人们关注,2000多年前的《神农本草经》就将之列为中药上品,杜仲具有降血压、补肝肾、强筋骨、抗衰老、抗肿瘤等功效。近来的研究证实杜仲叶与皮的化学成分基本一致,其中绿原酸(Chlorogenic acid)是杜仲起药理作用的主要有效成分之一[1-2]。因此,和金银花、杜仲皮等原料比较,从廉价的杜仲叶中提取绿原酸是一种更为经济合理的工艺方法。绿原酸的分析检测方法包括薄层扫描法、导数极谱法、紫外分光光度法、化学发光分析法、气相色谱法、高效液相色谱法等多种分析方法[3-6]。现有的绿原酸定量分析大多需要专门的分析仪器设备,对于实验室一般经常性分析来说,费用过高而且不及时,因此非常有必要寻找一种依靠简单仪器和适合基层操作的快速、准确的检测分析方法。 本文在前人工作的基础上,利用绿原酸和铝离子的络合显色反应,采用可见分光光度法测定杜仲叶中的绿原酸。该方法仪器简单、方法简便、结果准确,满足了实验室和生产常规分析检测的需要。 1材料与方法 1.1 测定原理 根据绿原酸类物质在碱性条件下与铝离子形成稳定的紫红色络合物,并产生特征吸收光谱而进行测定。反应式如图1所示。
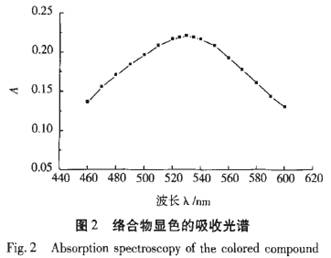
1.2主要仪器和试剂 1.2.1 主要仪器 721型分光光度计(上海分析仪器三厂); 紫外分析仪(上海顾村电光仪器厂)。 1.2.2主要试剂及标准溶液的配制 硝酸铝、亚硝酸钠、乙醇、氢氧化钠均为分析纯。 杜仲叶采自湖北五峰县。 绿原酸标样(中国药品生物制品检定所)。 绿原酸标准溶液:用分析天平准确称取绿原酸标准品0.0100 g,用95%乙醇溶解于500 mL的容量瓶中并定容,配制2×10-2g・L-1的绿原酸标准溶液。 1.3绿原酸溶液吸光度测定 取绿原酸标准溶液~定体积于10 mL容量瓶中,加入0.5 mL 5%的NaN0,和0.5 mL 10%的Al(N03)3静置5 min,再加人2 mL 1 mol・L-1的NaoH溶液并用体积分数95%乙醇定容,以95%乙醇作空白溶液,在530 nm处测定吸光度A。 1.4杜仲叶预处理及绿原酸量测定 准确称取10.0 g杜仲叶,用40%乙醇溶液按料液比为1:14,在80℃下回流提取150 min,重复提取3次。通过薄层色谱分析,在紫外分析仪下观察荧光现象,发现第3次提取液中显示绿原酸的蓝色荧光非常暗淡,说明从杜仲叶中第3次提取的绿原酸含量非常低。因此合并第1次和第2次提取液,将提取液浓缩定容于200 mL容量瓶中。吸取100 uL提取液,点样于20 cm×10 cm硅胶G薄层板上成2 cm均匀带状,用v(乙酸乙酯):v(甲醇):v(水)=10:4:3作展开剂,按常规操作展开。风干薄板,划出与标准品相同位置展开点的谱带,刮下吸收带部分的硅胶置于50 mL锥形瓶中,用10 mL体积分数80%乙醇溶液洗脱30min,将洗脱液定容至20 mL,分别量取绿原酸样品溶液1.0,2.0,3.0,4.0,5.0mL于10 mL容量瓶中定容,按1.3方法显色并测量吸光度A,计算杜仲叶样品中绿原酸的含量。 2结果与讨论 2.1 络合物显色的吸收光谱 配制一定浓度的绿原酸标准溶液,按1.3实验方法操作,吸光度A结果见图2。由图2可见,吸收峰在530 nm处最大,因此选用530 nm为测定波长。
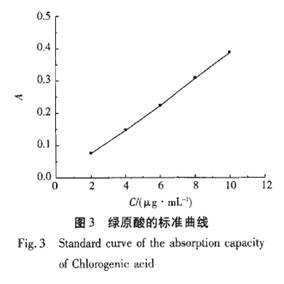
2.2绿原酸标准曲线的绘制 精确吸取绿原酸标准溶液1.0,2.0,3.0,4.0,5.0 mL,分别按1.3方法显色并定容至10 mL,在530 nm处测量吸光度。将吸光度4值对绿原酸的质量浓度c值进行线性回归,得回归方程为A=0.000 392 C一0.006 7,r=0.999 5,绿原酸质量浓度在1.7×10-4~1.0×10-2g・L一之问线性关系良好,结果如图3所示。 2.3显色溶剂的选择 实验表明,当绿原酸溶液用量、显色剂用量和操作条件都相同时,分别用蒸馏水和95%乙醇做显色溶剂,两种显色溶液的初始吸光度无大的差别。但是用95%乙醇显色的溶液,其吸光度能够保持更长的时间不变化,说明乙醇对显色化合物具有稳定作用,显色化合物的吸光度在1 h内无变化,完全能够满足测定的要求。
2.4络合显色剂用量的确定 绿原酸质量浓度在1.0×10-2g・L-1以内时,向溶液中加入5%的NaNO2和10%的A1(NO3)3溶液各0.5mL,溶液中的绿原酸可完全形成稳定的紫红色络合物。A13+为配合物的中心离子,AJ(No3)3的适宜加入量为0.5 mL,较少时吸光度偏低,较多时则影响不大。NaN02用作还原剂,以防止绿原酸被氧化。 2.5络合显色时间的选择 随着温度升高,显色时间明显缩短。在25℃,35℃,50℃的水浴中,络合显色反应达到稳定的时间分别为5,3,1 min。由于显色反应在室温下就能在较短的时间内完成,故选择室温下显色5 min。 2.6薄层层析展开剂的选择 对杜仲叶提取液的薄层分离展开剂进行了不同组成和配比的对比实验分析,其中以v(乙酸乙酯):v(甲醇):v(水)=10:4:3分离效果最好,可使绿原酸与干扰物质完全分离,Rf值0.65,薄层层析示意图如图4所示。
2.7精确度与回收率 取夏天和秋天采摘的杜仲叶各10.0 g,按1.4实验方法操作,测定杜仲叶中绿原酸的量,并计算相对标准偏差(RSD)。加标回收实验。量取浓缩后的杜仲叶样品溶液5.0 mL,加入一定量的绿原酸标准品,定容于10mL容量瓶中。吸取100仙L提取液,点样于薄板上成均匀带状,按常规操作展开。风干薄板,刮下吸收带部分的硅胶,用10 mL体积分数80%乙醇溶液洗脱30 min,将洗脱液定容至20 mL,分别量取溶液1.0,2.0,3.0mL于10 mL容量瓶中定容,按1.3方法显色并测量吸光度A,计算加标后样品中绿原酸的量以及加标回收率。
3 结论 绿原酸在碱性条件下可与铝离子形成稳定的紫红色络合物,并产生特征吸收光谱。采用721型可见分光光度计对杜仲叶中的绿原酸质量浓度进行分析测定,仪器简单、方法实用、结果准确。实验确定显色化合物最大吸收波长为530 nm,绿原酸标准曲线回归方程为4=0.000 392 c―0.006 7(r=0.999 5),绿原酸质量浓度在1.7×10-4g・L-1~1.0×10-2g・L-1之间线性关系良好。 参考文献: [1] 赵玉英,耿权,程铁民.杜仲化学成分研究概况[J].天然产物研究与开发,1995,7(5):46―52. [2] 曲保雪,朱立红,芦春莲.杜仲产品加工利用现状与进展[J],河北林果研究,2001,16(4):387-391. [3] 王丽,帅琴,汤志勇,等.茶叶样品中绿原酸含量的高效液相色谱测定[J].分析测试学报,2001,20(1):76-78. [4] 聂丽萍,左兴华.薄层扫描法测定清热颗粒中绿原酸的含量[J].河北中医药学报,2002,17(3):27-28. [5]李自林,郑筱梅,王琰.绿原酸的导数极谱法测定[J].化学研究与应用,1998,18(1):199―202. [6]刘圣金,狄留庆,吴德康,等,高效液相色谱法测定杜仲中绿原酸的含量[J].中国中医药信息杂志,2006,13(1):44_45. 产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸 上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 可见分光光度法测定杜仲叶中的绿原酸
可见分光光度法测定杜仲叶中的绿原酸