| 苦丁茶中熊果酸的分离纯化研究 |
| 发布时间:2010-09-30 信息来源:admin 发布人:admin 点击次数:3010 |
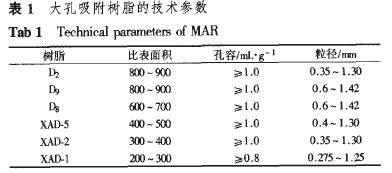
任秀莲1,2,周春山1,魏琦峰1,2,肖建波1,雷启福1,汤小胜1(1.中南大学化学化工学院,湖南长沙410083;2.内蒙古科技大学化学化工学院,内蒙古包头014030) 摘要:目的研究苦丁茶(llex kudlingcha C.J.Tseng)中熊果酸的分离纯化,建立分离纯化工艺条件,以利于苦丁茶资源的开发利用。方法以熊果酸浸出率为考核指标,采用正交实验法考察诸因素对浸出率的影响。乙醇提取液经沉淀富集和大孔树脂柱色谱纯化得到熊果酸,采用HPLC分析检测。结果优化的提取条件为:在85%水浴中,以体积分数90%乙醇水溶液为提取溶剂,固液比为1:14,提取2次,每次提取2.5 h,熊果酸的浸出率可达到1.44%。98树脂分离富集的最优条件:样品溶液熊果酸浓度l~2mg・mL-1,样品溶液pH=6.0~7.0,吸附l h,洗脱剂pH=11.0,依次用水、4倍体积30%乙醇、4倍体积90%乙醇以2~3 mL・min-1的流速洗脱,收集90%乙醇洗脱液,熊果酸回收率为97.82%,纯度为95.O%。结论该工艺产品纯度高,收率高,可实现工业化。 关键词:苦丁茶;分离;纯化;熊果酸;大孔吸附树脂;高效液相色谱法 熊果酸(ursolic acid,UA)是一种弱极性的五环三萜酸,具有明显抗炎、降脂、降酶和抗癌作用,是近年新发现的抗癌活性成分,也是现代肿瘤药物筛选的新热点[1]。目前,熊果酸的提取分离主要采用有机溶剂萃取和硅胶柱色谱分步洗脱的方法[2~4],这些方法的工艺流程长,收率低,且使用有毒有机溶剂。近年来,大孔吸附树脂在药物提取分离中显示出越来越重要的作用[5~6],尤其对非极性或弱极性化合物具有良好的吸附分离性能,因此,作者采用大孔吸附树脂(macro-po.rOllS adsorption rosin,MAR)对苦丁茶中的熊果酸进行了分离富集研究,为熊果酸的分离富集开辟新路,对熊果酸工业化生产有一定的指导意义。 1材料、试剂与仪器 1.1材料、试剂 苦丁茶,2002年采摘,广西;50℃下烘干粉碎备用;药材经广西中医学院药学院中药鉴定室鉴定为:冬青科植物苦丁茶(//ex kud/ngcha c.J.Tseng),药材符合2000年版(一部)有关项下的规定。乙醇、甲醇、氢氧化钠、硫酸等为分析纯;熊果酸标准品(Sigma公司,纯度为97%);6种非极性大孔吸附树脂(南开大学化工厂)的物理结构参数见表1。
1.2仪器
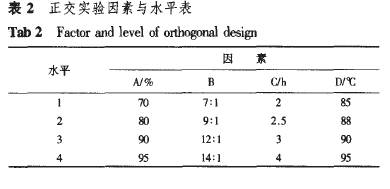
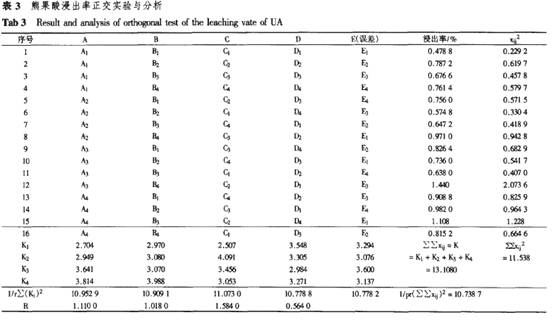
Err 8100 HPLC.pump(Biotronik);BT 8200 HPLC Uv/ⅥS Detector(Biotronik);C.R3A Chromatopac(Biotronik)。 2方法 2.1标准溶液的配制 准确称取熊果酸标准品,用甲醇溶解后配制成浓度为0.804 0 mg・mL~,作为测定样品的标准溶液。 2.2色谱条件 Hypersil C18色谱柱(10 gm,250 toni×4.6 mm),流动相:甲醇.水.乙酸(90:10:0.02),微滤膜过滤流动相后,超声波脱气处理20 min;检测波长220 nm;灵敏度0.08AUFS;流速0.6 mL・min~;温度为25℃。 2.3标准曲线的绘制 准确移取0.804 0 mg・mL“的熊果酸标准溶液0,2.0,4.0,6.0,8.0和10.0 mL,甲醇定容至10 mL,配制成标准系列。在“2.2”项色谱条件下,吸取上述溶液,分别进样6血,每一个浓度重复测定6次。以浓度C(mg・mL。)为横坐标,峰面积A为纵坐标进行线性回归,得到如下回归方程:A=524 170c~902.5,R2=0.999 8。 2.4样品的测定 样品在与标准曲线相同的色谱条件下测定,根据回归方程得到样品中熊果酸的浓度。 2.5检测样品的制备 将分步洗脱得到的洗脱液减压浓缩至干,甲醇溶解,稀释定容至10 mL,按“2.4”项下检测,外标法定量。 2.6大孔吸附树脂的预处理 先用乙醇充分浸泡溶涨大孔吸附树脂,然后以蒸馏水洗至无混浊现象,再用4%HCI浸泡,蒸馏水洗至无Q~存在为止。在50℃真空干燥1 d,备用。 3结果与讨论 3.1正交实验 根据单因素实验结果"1得出:乙醇体积分数(A)、液固比(B)、提取时间(c)和提取次数都不同程度地影响着熊果酸的浸出率。当提取次数达到3次后,浸出率变化不大。而且在实际生产中也不可能进行多次提取,因此选择的回流提取次数为2次。不同的水浴温度(D)可以使提取液的回流速度不同,从而影响浸出率。因此正交实验以乙醇体积分数、液固比、提取时间和提取温度4因素确定[8],正交实验因素与水平选择见表2,熊果酸浸出率的正交实验及计算结果见表3。方差分析见表4。
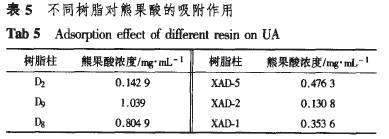
从表3,4可知,提取时间显著影响熊果酸的浸出率,乙醇体积数和液固比对浸出率有一定的影响,提取温度在85~95℃范围内对浸出率没有明显影响。由正交实验结果可以得到最佳提取条件为A3&C2 Dl,即乙醇体积分数为90%,液固比为14.回流时间为2.5 h,回流温度为85℃。在该条件下,熊果酸的浸出率可达到1.44%。 3.2熊果酸的富集 “3.1”项下苦丁茶提取液用20%NaOH调节溶液的pH=9~11,除去大分子杂质,所得滤液用10%飓s04酸化至pH=1。2,过滤所得沉淀,水洗至近中性,50℃真空干燥,得到熊果酸富集物。、采用“2.4”项下方法分析其中的熊果酸纯度为28.05%。 3.3大孔吸附树脂对熊果酸吸附性能的研究 3.3.1大孔吸附树脂对熊果酸的静态吸附性能分别称取6种大孔吸附树脂8 g,按“2.6”项下方法对树脂进行预处理,湿法装柱。甲醇溶解熊果酸富集物,浓度为1.3l mg・ml-1,再用极性调节剂以1:1稀释后上柱,静态吸附1 h后,先以H20洗至无色,再以90%乙醇洗脱至无三萜反应[9],按“2.5”项下方法处理洗脱液,结果见表5。
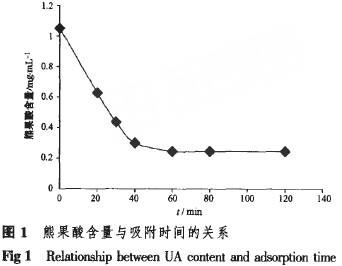
从表5可知,D8,聩树脂对熊果酸的吸附量较高,而XAI)-2树脂最低,但试验表明:XAD-2树脂吸附杂质的能力很强,而XAD-5,XAD-I树脂对熊果酸的吸附能力较强,90%乙醇洗脱时很难使熊果酸解吸完全,洗脱速度明显比其它4种树脂慢。因此,选择聩,马树脂富集熊果酸,XAD-2树脂纯化熊果酸进行研究。从几种树脂的主要技术参数分析,粒径为0.6~1.42 mm的树脂适合于富集熊果酸,而粒径为0.35~1.30 mm的树脂不适合于富集熊果酸。 3.3.2洗脱剂种类的选择根据绿色清洁工艺的要求,采用乙醇.水体系为洗脱剂不仅避免了以往硅胶柱色谱富集熊果酸时有毒有机溶剂的使用,而且乙醇回收后可以重复使用,降低了生产成本,为产品的产业化开发提供了保证。因此,本研究选用乙醇一水为洗脱剂。 3.3.3吸附时间的确定精确称取经预处理活化的D8大孔 吸附树脂1.000 g于100 mL烧杯中,以熊果酸含量为1.05mg・mL。1的样品30 mL加入到烧杯中,吸附20,30,45,60,90和120 min后依次取样,按“2.4”项下分析方法检测,结果见图1。
由图1可知,20 min以前吸附速度较快,随着吸附时间的延长,吸附速度越来越慢,直到平衡,所以吸附时间以1 h为宜。 3.3.4洗脱剂浓度的选择域树脂8 g,按“3.3.1”项下方法吸附后,采用水、10%乙醇、30%乙醇、50%乙醇、70%乙醇、90%乙醇各200 mL分步洗脱,收集洗脱液,按“2.5”及“2.4”项下的方法制备样品与测定,结果见表6。
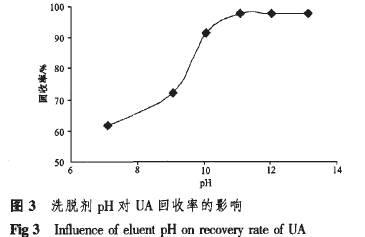
由表6可知,水一30%乙醇不能洗脱熊果酸。随着洗脱剂乙醇体积分数的增大,洗脱能力逐渐增强,70%乙醇对熊果酸有一定的洗脱能力,90%乙醇的洗脱能力最强,为70%乙醇洗脱剂的5倍。在洗脱过程中。如果洗脱剂分子与吸附树脂的亲合力大于目标物质与吸附树脂的亲和力,就可以将该目标物质置换而洗脱下来。因此,洗脱时,先用与吸附剂亲合力小的溶剂,然后逐渐改变洗脱剂的极性,将与吸附剂亲和力更强的物质洗脱下来,以达到良好的分离效果。本实验采用D型非极性大孔吸附树脂为吸附剂,乙醇.水为洗脱剂,因此,洗脱剂的极性越强,洗脱能力越弱;洗脱剂的极性越弱,洗脱能力越强。这与高效液相色谱检测所选流动相的组成是一致的。 3.3.5样品溶液pH的选择甲醇溶解熊果酸富集物,再用极性调节剂以1:I稀释,分别调节样品溶液的pH为2.87,4.64,7.07,9.23,II.25后,D8树脂柱静态吸附l h,水洗至无色,30%乙醇、90%乙醇各200 mL洗脱,收集90%乙醇洗脱液,洗脱液按“2.5”项下方法处理,结果见图2。 从图2可以看出,当样品溶液的pn=7.07时,树脂对熊果酸的吸附量最大,柱后流出液中熊果酸的含量最小,因此,选择样品溶液pH为6―7有利于熊果酸的吸附。当pH> 7.07时,熊果酸的吸附量逐渐下降,主要是因为熊果酸酸根离子的浓度增大,从而增大了熊果酸在洗脱剂中的溶解度,减小了与大孔吸附树脂的作用力,不利于吸附。实验中观察到,当样品溶液的pH为2.87,4.64时,水洗脱时有三萜酸沉淀析出,因此,酸度过低也不利于熊果酸的吸附。 3.3.6洗脱剂pH的选择平行装5根D8树脂柱分别命名为1,2,3,4,5,取浓度为1.31 nag・mL“熊果酸富集物溶液10.00 mL,10.00 mL极性调节剂稀释后,调节pn=6.58,上样,静态吸附1 h后,分别水洗至无色,30%乙醇200 mL洗脱,再分别用pH=7,9,10,11,12,13的90%乙醇洗脱剂200mL洗脱至无三萜反应,控制洗脱流速为2―3 mL・min~,将90%乙醇洗脱液酸化至pn:4.0,过滤,所得沉淀水洗至中性后,甲醇溶解定容至10.00 mL,按“2.4”项下分析方法检测,外标法定量,结果见图3。
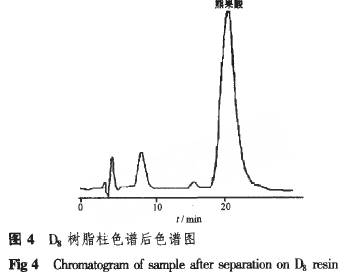
由图3可知,洗脱剂pH对洗脱能力有显著的影响u[10]。随着洗脱剂碱性的增强,洗脱能力逐渐增强,当洗脱剂pH≥11时,洗脱能力达到最大值。因此,选择洗脱剂pH=11为宜。这是因为,通过改变洗脱剂pH值,使熊果酸以离子型存在,很容易被洗脱下来,从而提高了洗脱率。当洗脱剂pH≥11时,熊果酸的回收率可达gr7.82%,纯度可达95.0%。 “2.4”项下色谱条件下,对D8树脂吸附后的产品进行分析,结果见图4。可见,D8树脂可以有效地纯化熊果酸。采用XAD-2树脂进一步进行纯化可以获得更高纯度的产品。
4结论 在85℃水浴中,以体积分数90%乙醇水溶液为提取溶剂,固液比为l:14,提取2次,每次提取2.5 h,熊果酸的浸出率可达到1.44%。大孔吸附树脂可以成功应用于苦丁茶中熊果酸的分离与富集,可以大幅度地提高熊果酸的收率和纯度。乙醇.水洗脱液的使用避免了传统工艺中有毒有机溶剂引起的2次污染,使分离纯化工艺安全、高效和低成本。pH对熊果酸在大孔吸附树脂上的吸附与洗脱有明显的影响,通过调节pH=6~7,可以成功使熊果酸吸附,调节pH≥ll可使熊果酸洗脱完全。 参考文献 [1] 黄镜,孙燕.熊果酸抗肿瘤活性[J].中国新药杂志,1997,6(2):101. [2] 樊文明,边专,王茜,等.从女贞叶中提取熊果酸的方法[P].中国专利:1358733A,2002-07.17. [3] 文永新,陈秀珍,金静兰.苦丁茶化学成分的研究[J].广西植物,1990,10(4):364. [4] 李晓蒙.小叶女贞化学成分研究[J].广西药学院学报,1998。14(2):93. [5J Jahan N,Almed w,Malik A.A lupene-type triterpene from Mknasopselengi[J].Phytochem础ry,1995,39(1):255. [6] 张红,柳正良,王洪泉.大孔吸附树脂在药学领域的应用[J].中国医药工业杂志,2001,32(1):41. [7] 任秀莲,钟世安,周春山,等.苦丁茶中熊果酸的提取工艺[J].中南大学学报(自然科学版),2004,35(1):70. [8] 郑用熙.分析化学中的数理统计方法[M].北京:科学出版社.1986:180―206. [9] 姚新生.天然药物化学[M].第3版.北京:人民卫生出版社.2001:276. [10] 刘斌,石任兵,余超.影响大孔吸附树脂分离草药化学成分的因素[J].中草药,2002,33(5):475. 产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸 上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 苦丁茶中熊果酸的分离纯化研究
苦丁茶中熊果酸的分离纯化研究