| 杜仲颗粒中绿原酸含量测定的研究 |
| 发布时间:2010-09-21 信息来源:admin 发布人:admin 点击次数:2686 |
杜仲颗粒收载于《中华人民共和国卫生部药品标准》(中药成方制剂)第十册(编号:WS3一B一1938-95)。由杜仲、杜仲叶2味药组成,具补肝肾,强筋骨,安胎,降血压之功效,临床上用于肾虚腰痛,腰膝无力,胎动不安,先兆流产,高血压症。原质量标准中,未对成品进行含量控制。文献报道[1,2,3,4]。 ,杜仲的化学成分主要含木脂素类、环烯醚萜类及杜仲胶等,杜仲叶含木脂素类、环烯醚萜类、苯丙素类化合物、黄酮类、氨基酸及微量元素等成分,其中二者均含有绿原酸,绿原酸含量测定方法有薄层扫描法[5,6,7 ]、高效液相色谱法[8,9,10]等。本文采用HPLC法测定杜仲颗粒中绿原酸含量,为该制剂质量标准的改进提供实验依据。
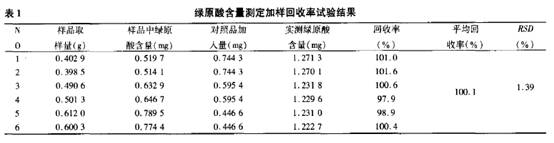
l.仪器与试药 岛津公司LC.2010A高效液相色谱仪,SPD.川OAvp二极管阵列检测器,CLASS・VP色谱工作站,sartoriusBP211D电子天平(北京赛多利斯天平有限公司)。绿原酸对照品(110753200212,中国药品生物制品检定所);乙腈为色谱纯,水为重蒸馏水,其余为分析纯;样品:杜仲颗粒(批号:040401、040601、040602、040603,某有限责任公司)。 2.方法与结果 2.1 色谱备件 色谱柱:Shim―pack VP―ODS(4.6 mm×150 mm,5 m);流动相:乙腈-0.4%磷酸溶液(9:91);流速:1.0 ml/min:柱温:35。C;枪测波长:327 nm。结果:绿原酸峰与相邻峰的分离度大于1.5,峰形对称,理论板数以绿原酸峰计算大于2500。缺绿原酸阴性对照无干扰。 2.2 溶液的制备 2.2.1 对照品溶液的制备精密称取绿原酸对照品适量,加50%甲醇制成每l mL含50 mg的溶液,即得。 2.2.2 供试品溶液的制备取本品,研细,取1.0 g,精密称定,置25 mL量瓶中,加50% 甲醇约2O mL,超声处理(功率150 W,频率50 KHz)30 rain,放冷,用50%甲醇稀释至刻度,摇匀,滤过,取续滤液,离心,即得。 2.2.3 缺绿原酸阴性对照溶液的制备取缺绿原酸阴性对照样品,按供试品溶液的制备方法制备,即得。 2.3 线性关系精密称取绿原酸对照品l3.35 mg,置25mL量瓶中,加50% 甲醇溶解并稀释至刻度,摇匀,精密吸取1.5 mL置10 mL量瓶,作为对照品溶液;分别精密吸取此对照品溶液1,2,4,10,16μl ,按上述色谱条件进行分析,测定峰面积,以进样量x( g)对峰面积Y进行线性回归,得回归方程为:Y=2.181 0×10 X一2.119 9×10 ,r=0.999 9;表明绿原酸在0.08一1.28 g之间呈良好的线性。 2,4 精密度试验分别精密吸取对照品溶液与供试品溶液(批号040401)各10.0μl,按上述色谱条件连续进样5次,测定峰面积。结果对照品RSD =1.46%,样品RSD=1.28% 。 2.5 稳定性试验取样品(批号040401)适量,按供试液制备方法制备供试液,与上述对照品溶液于0,1,2,4,8,16 h分别精密吸取10.0μl ,按上述色谱条件测定。结果对照品RSD=0.88% ,样品RSD=1.94% 。表明对照品溶液、样品溶液在16 h内测定基本稳定 2.6 重复性试验取样品(批号040401)1.0 g共5份,按样品分析方法进行测定,测得平均含量为0.129%,RSD:1.68%。 2.7 加样回收率试验取样品(批号040401)适量,6份,分别加入一定量的绿原酸对照品(C=0.2977 mg/mL)1.5,2,2.5 ml ,按样品分析方法进行处理,并各平行测定2次,结果见表1,如表所示。本方法加样回收平均回收率为100.1%,RSD:1.39%。表明回收率的重现性较好。 3 样品测定 按上述色谱条件,对3批样品(批号:040601、040602、040603)进行测定,结果本品每l g颗粒含绿原酸(c.6 H.09)分别为0.93,1.18,1.07 mg。
4 讨论 4.1 指标成分的选择目前,绿原酸含量测定较多,但尚无杜仲颗粒中有关绿原酸含量测定的文献报道。《中国药典》2000年版一部杜仲项下收载了有关含量浸0定,但经多方联系无法购买到供含量测定用对照品:松脂醇二葡萄糖苷。经文献查阅,杜仲、杜仲叶中均含绿原酸,经上网查询⋯ ,《中国药典)2005年版一部将收载杜仲叶绿原酸含量测定方法,故选择绿原酸作为指标成分进行含量控制。阴性选用缺杜仲、杜仲叶样品。 4.2 检测波长的选择实验曾对绿原酸对照品及供试品色谱叶1绿原酸峰在SPD―M10Avp二极管阵列检测器上进行扫描,结果:二者均在327 nm波长处有最大吸收,实验选择327nm作为检测波长。 4.3 流动相的选择实验曾以叶=I醇一水一甲酸(30:70:1)、乙腈一2% 乙酸(15:85)、乙腈旬.4%磷酸溶液(15:85)、乙腈一0、4%磷酸溶液(9:91)为流动相,流速:1 mL/min,以Shim―pack VP―ODS柱为分析柱,桂温35。C,进行试验研究,结果前i个条件均未达到满意的分离效果;而最后一个条件中绿原酸峰已达基线分离,绿原酸峰虽略拖尾,但小影响最后分析结果;缺杜仲及杜仲叶阴性埘照样品均无干扰。实验最终选用乙睛-().4%磷酸溶液(9:91)为流动卡H,流速1.0 mL/min,十}温:35。C 4 4 分析柱的选择实验发现色潜柱埘样品巾绿原酸的分离仃较大影响,曾用Diamonsil(钻石)C,住(4.6 mm×150mm,5 m)Lj Kromasil Cl H柱(4.6 mill×150 mm,5 m)柱,以乙腈旬.4%磷酸溶液(9:91)为流动桐,二者均未达到满意的分离效果,绿原酸峰与相邻峰末达到基线分离,后以Shim―pack VP―O1)S(4.6 mm×l50 mm,5 m)作为分析柱,结果绿 原酸峰与桐邻峰分离度大于1.5,理论塔板数以绿原酸峰计算均大于2500。方法学研究实验选用Shim-pack VP―ODS(4.6 mill×150 mm,5 Ixm)色谱柱。 4.5 提取条件的选择供试液制备中,对提取溶剂(甲醇、乙醇、50%甲醇),提取方法(回流、超声),提取时间(15、30、45 min)进行了考察。结果用50% 甲醇超声处理30 min为最佳提取条件。
参考文献: [1] 刘影秋.杜仲的化学成分及应用研究进展[J].贵卅I农业科学.1996.6:58-6O. [2] 管淑玉,苏薇薇.杜仲化学成分与药理研究进展[J].中药材,2003,26(2):124―129. [3] 晏嫒,郭丹.杜仲叶的化学成分及药理活性研究进展[J].中成药,2003,25(6):491-492. [4] 赖娟华,徐丽瑛,饶华,等.杜仲叶化学成分和药理作用研究概况[J].1i ra成药,2004,4(2):67-69. [5] 原源、袁继民、赵庆华.薄层扣描法测定健肝I号台齐lJ中的绿原酸含量[J].解放军药学学报,2002,18(4):237 238. [6] 王瑞明,靳秋萍,郝旭亮,等.薄层扫描法测定f_1腔宅中绿原酸含晕[J]时珍国医国药,2003,14(6):334―335. [7] 聂丽萍,左兴华,薄层扫描法测定清热颗粒中绿原酸的含量[J].河北中医药学报,2002,17(3):27 28. [8] 董林,李毅,邛晓鸿.银柴颗粒匝量标准研究[J],中成药,2004,26(1):29 32. [9] 倪健,任天池.健脾降脂颗粒中绿原酸的含量测定l Jj.北京中医药大学学报,2003,26(2):50-52. [10] 罗杰,杨东升,欧阳慧芳,等.El炎清颗粒(无糖型)中绿原酸的含量测定[J].中国中药杂志,2003,28(8):780 781 [lI] 中闰药典2005年版内容公示.http://www.chp.org on/2005gs/zl/gsz1.him.
产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸
上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 杜仲颗粒中绿原酸含量测定的研究
杜仲颗粒中绿原酸含量测定的研究