| ��������������ȡɽ���Ƿ��Ͳ����е��ܹ��� |
| ����ʱ��:2010-09-04 ��Ϣ��Դ:admin ������:admin �������:5047 |
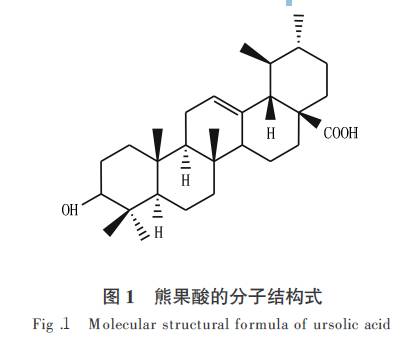
����Σ� , �ι��죱 , �������� , �ں����� , �����٣� (�� . �㽭��ѧ����ϵͳ������ʳƷ��ѧѧԺʳƷ��ѧ��Ӫ��ϵ, �㽭���ݣ����������� ; �� . ������ҩƷ������,�㽭���ݣ����������� ;�� . �㽭��ҵ��ѧҩѧԺ,�㽭���ݣ����������� ) ժ��Ҫ:���ó�������������ȡɽ���Ƿ��Ͳ����е��ܹ���,��HPLC ���ⶨ�ܹ��Ậ��,���о��ܹ�����ȡ����ѹ�������.�ڣ��� �� ��,��ĸ��������ԭ��������Ϊ�� �� ���� ,ҡ��ת��Ϊ������ r��min�� �� ʱ����Ч����,����ʱ���;�ھƾ�Ũ�ȣ����� ,�¶ȣ��� �� ,�������ʣ����� W ,ʱ�䣳�� min ����������ȡЧ�����,�ܹ������Ϊ��.���������� . �ء�������: ɽ����; �ܹ���; ����; ��ȡ ɽ����( Cornus o f f icinalis Sieb . etZucc) ��ɽ����ϵɽ���ǿ�ֲ��,��һ����Ҫ��Ұ����Դ.�����ζ�ᡢɬ,��,�������,�в��������ɬ�����ѵĹ�Ч, ����ҽ�ٴ����õĴ�ͳ��˥��ҩ��֮һ, ��Ҫ���ܳɷ�Ϊ��ϩ�����ࡢ���ա����ǡ��ܹ��ᡢ��չ��ᡢ���ʵ�[ ��] . �ܹ���( ursolie acid ,UA) ,��һ�������Ե��廷������,�����ʽΪC���� H���� O�� (ͼ��)[�� ] ,������Ϊ������.���� ,�ܵ㣲���� �� ������ �� ,�����ڶ������������,�����ڼ״����Ҵ�������,�����ڱ�ͪ,���ڱ����ȷ¡�����,������ˮ��ʯ����.�о�����,�ܹ�����нϸߵ�����ѧ����,�����������Ը����˵ı������������Ϳ�����������[�� ] .�ܹ�����нϸߵ�ҽ�ü�ֵ�ͱ�������,�й������г�ǰ��,�����ܹ������ȡԽ��Խ�ܵ�������ѧ�ߵĹ�ע.
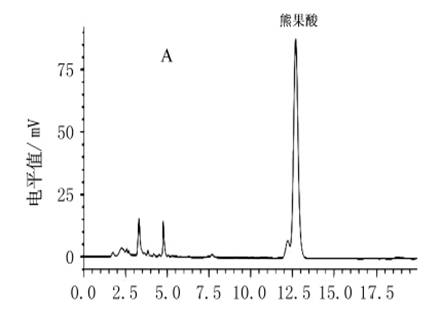
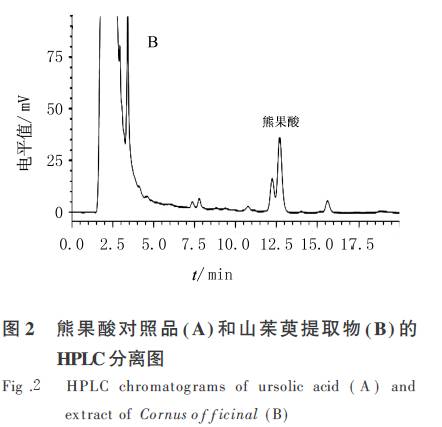
ɽ�������ܹ������ȡ�����ж���,��������ȡ������������ȡ�����Ҵ�������ȡ�������ٽ�������ȡ��( SFE) ��.���г�������ȡ�������ó�����ǿ��Ŀջ�����ʹϸ��������,ǿ������,����������ܹ������ȡЧ��.��ԭ���м����ĸ��,������ͽ��Ƿֵ��ص�[�� ] ,�ֽ�ɽ�����е�����,�������Ӱ����ȡ���̼�Ч�ʵ�����.�����ܹ�����������,�������ĸ���Ͷ�Ӱ����ʺ�����.����ɽ�����е��Ƿ�,�������Լ���ȡ����,���һ�������ߴ��������ܹ���ĺ���.����Ϊֹ,�йؽ�ĸ���ǽ�ϳ�����������ȡ����Ӧ����ɽ�������ܹ�����ȡ��δ�����ױ���. �� �������뷽�� 1.1 ���ġ��� ɽ���Ǹ����ʵ�����㽭ʡ�ٰ���,�ɺ�����Ŀ����Ƽ�����˾�ṩ.��ƽ�ĸ( Saccharomyces cerev isiae ) , �ɰ�����ĸ�ɷ�����˾����;�ܹ������Ʒ�����й�ҩƷ������Ʒ������;�״�Ϊ����ɫ�״�,�����Ϊ����������. 1.2 ���ǡ��� KYC������B ��ҡ��(�Ϻ�����ʵ���豸����˾) ;WYT ��������(����ʡȪ�������ʵ�������豸����˾) ;KQ��������DB �����س���������(����ʡ��������ɽ��(��)������������˾) ;����LC�\����A ��ЧҺ��ɫ����(�ձ�����˾) ;DZX�\�������� ��ո�����(�Ϻ�����ʵ���豸����˾) . 1.3 �������� 1.3.1 ��ɽ������ȡ�������̡���ɽ���ǽ�(ɽ���Ǹɷۣ� ˮ) ���ͳ��ǼӾƾ�������ȡ����(��ȥ����) Ũ����ѹ�������Ʒ. 1.3.2 ������Ԥ���� 1.3.2.1 ��ɽ���Ƿ���. ��ȡ���� g �������ɽ���Ǹ����ʵ,��������ƿ��,���룴�� mL ˮ,����,��ˮԡ����. �ɽ�ĸ�:���趨����,��ȡһ�����ɽ�ĸ,���룱�� ��������ˮ,���� �� ���ȣ��� min ,ת�������� �� ��ˮԡ����,����ĸҺ����ȴ,ת������ƿ��,��ţƤֽ���ƿ��,����ҡ����,���趨�����·���. 1.3.2.2 ������Һ�Ƿֺ����ⶨ. ÿ������ h �������Ʋ�������Һ���Ƕ�,��¼����Һ�Ƕȵı仯. 1.3.2.3 ������������ѡ��. ��ʵ��Է����¶ȡ���ĸ��������ҡ��ת�ٽ��е�����̽��,�ֱ죳 �����ض�ԭ���������ǶȺͷ����ٶȵ�Ӱ��. 1.3.3 ��ɽ�������ܹ�����ȡ��������������Ϻ�,����Һ���룸���� mL ��ͬŨ�ȵľƾ�,���ڳ�����������,������ȡ�¶ȡ����������ʺ���ȡʱ��,��ȡҺ���˺����ڣ������� mL ������ƿ��. 1.3.4 ����ȡҺ���ܹ��Ậ���ⶨ 1.3.4.1 ��ɫ��������. ɫ����Hypersil C���� (����cm �� ��.�� mm ,������ ��m) ;������:�״��\ˮ�\����( ���� �� ���� �� ��.�� ) ;��Ⲩ�������� nm ,���٣�.��mL��min�� �� ;����:����.�ܹ������Ʒ��ɽ���ǵ�HPLC ͼ��ͼ�� ,���ӻ�����Ϊ����.���� .
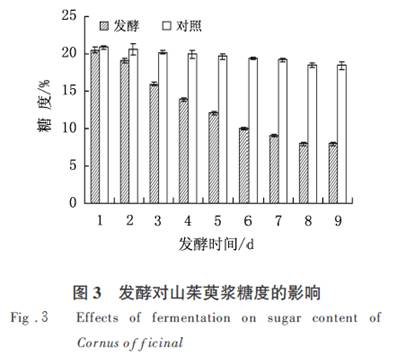
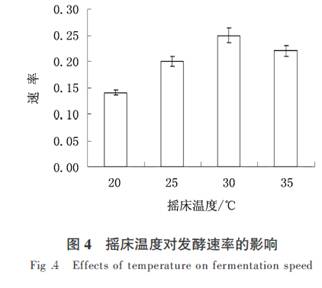
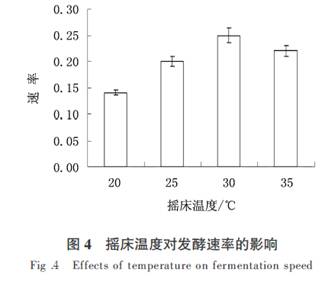
1.3.4.2 ������Ʒ��Һ�Ʊ�. ���ܳ�ȡ���������ص��ܹ������Ʒ�� mg ,��ɫ�״��״��ܽ�,��Һ���ܹ�������Ũ��Ϊ�� mg��mL ���� ,����Ĥ����,���ڱ�������ر���,����. 1.3.4.3 ����ƷҺ�Ʊ�.ȡ�� mL ���ݺ����ȡҺ,��ɫ�״��״�ϡ�������� mL ,����Ĥ����,��Ϊ����Ʒ��Һ. 1.3.5 ���������鷽����ơ�����Ԥ��ʵ��Ļ�����ѡȡ���ܹ��������Ӱ��ϴ�ģ������ؽ�����������:�ƾ�Ũ��,��������ȡ�¶�,����������,��������ȡʱ��. 1.4 ���ܹ�����ʼ��� X �� ( A���� C��� V ) �� ( A��� Mԭ����) �� �������� ,ʽ��A��Ϊ����Ʒ�����;A��Ϊ����Ʒ�����;C��Ϊ��ƷŨ��;V Ϊ����Ʒ�ܽ����Һ���;Mԭ����Ϊɽ���Ǹɷ�����;X Ϊ�ܹ������/ �� . 1.5 �����ݴ��� ������ʵ��������Origin pro ��.�� �洦��,ʵ���ظ��� ��. �� ����������� 2.1 �����Ͷ�ɽ���ǽ��Ƕȵ�Ӱ�� ���ֽ�ĸ��ɽ���ǽ���,�ڽ�ĸ�������������½��з���.����ǰɽ���ǽ����Ƕ�Ϊ������ .��ͼ�� ��֪,�������Ƕ��淢��ʱ��仯������,���������ɽ���ǽ��Ƕȴӵڣ� d ��ʼ�仯����,���ڣ� d �仯������,�ڣ� d ���ڣ� d ��仯ά���ڽϸ�ˮƽ,���仯���������Լ���,�ڣ� ���� ��������Ƕȱ仯��������,ά���ڣ��� .�ɼ�ͨ�����������Խ���ɽ���ǽ����Ƕ�. 2.2 ������������ѡ�� ����������ѡ����Ҫͨ�������¶ȡ���������ҡ��ת�٣������ضԷ����ٶ�(�ã�/ T ��ʾ,T ������������)�ͷ���Һ�����Ƕȣ� ��ָ���Ӱ����ʵ��.����������,��ͬ���ʹ��������ǶȾ����ڣ��� ������ ֮��,�仯������. 2.2.1 �������¶ȵ�ѡ������ҡ��ת�٣����� r��min���� ,�������� �� ���� ,�Ƚ�ҡ���¶��ڣ��� ������ ������ �ͣ��� �� �µķ����ٶ�. �¶���Ӱ�췢�͵���Ҫ����֮һ,���ݷ��͵�һ����[�� ] ,��ijһ�¶ȷ�Χ��,�����ٶ�
���¶ȳ�����,ÿ���ӣ��� �� ,�����ٶȽ����ӣ���.���¶ȳ�����ĸ�����������¶�ʱ,���¶Խ�ĸ�������������������.��ͼ�� ��֪,�����ٶ�����ҡ���¶����������,������ �� ʱ�ﵽ���,�¶��ټ������ߵ����� �� ʱ,����������������.�ɼ���ҡ���¶���Ϊ���� �� ʱ�����¶Ƚӽ���ĸ���������¶�,�����������.
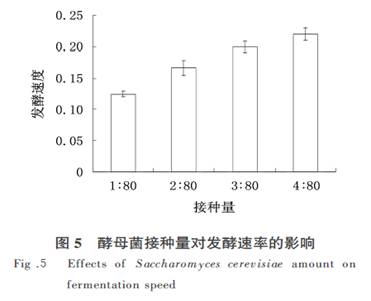
2.2.2 ����������ѡ�����Ʒ����¶ȣ����� ,ҡ��ת�٣����� r��min�� �� ,�����ĸ�������Է���ʱ���Ӱ��. ������������Ӱ���ĸ�����ٶȵ�����֮һ.��ĸ�����У� ��ʱ��,�������ڡ������ڡ��ȶ��ں�˥����,���г������Ƿַֽ����ʱȽϵ�,�ȶ������.���������Ķ���ֱ��Ӱ�쵽��ĸ���������ڵij���,������Խ�������Խ��,�����ȶ�������ʱ��Խ��,�ﵽ�Ƿ����ֽ���������ʱ���Խ��.��ͼ�� ��֪,�����������Ž����������Ӷ�����,�������ӵ�������С,��������Ϊ�� �� ���� �ͣ� �� ���� ʱ,�������ʲ���Ѿ�������.�ۺϿ���ʱ��ͳɱ��� ������,ѡ����������Ϊ�� �� ���� . 2.2.3 ��ҡ��ת�ٵ�ѡ�����Ʒ����¶ȣ����� ,�������� �� ���� ,����ҡ��ת�ٶԷ���ʱ���Ӱ��. ҡ��ת��Ҳ��Ӱ�췢�͵���Ҫ����֮һ.ҡ��ҡ���Է��͵�����Ӱ����Ҫ�У�������:
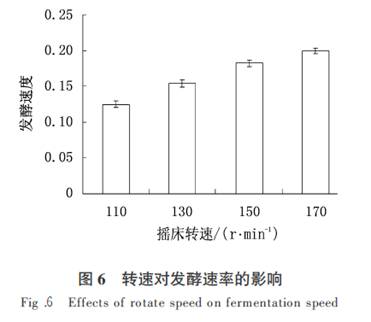
��һ��ͨ��ҡ��ҡ���ܹ�ʹ����Һ��������������,�����ڽ�ĸ��л,�����Ƿֽ���;�����ͨ��ҡ��ҡ���ܹ�ʹ��ĸ����뷢��Һ���,ʹ�����ӳ��.������ת��Խ�߷�������Խ��,�ڷ���Һ������������ͽ�ĸ������Һ��ϳ�ֵ�������,��ĸ�Ѿ��ﵽ��������״̬,����ת��,�������ʽ��������.��ͼ�� ��֪,������������ҡ��ת�����Ӷ�����,�������ӵ���������ƽ��.��ת�ٴӣ����� r��min�� �� ���ӵ������� r��min�� �� ʱ,�������ʵ������Ѳ�����.�ɼ�,ת�ٿ����ڣ����� r��min�� �� �����.
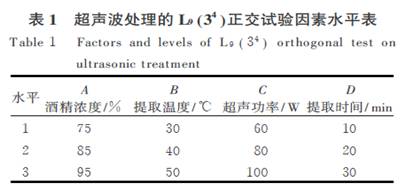
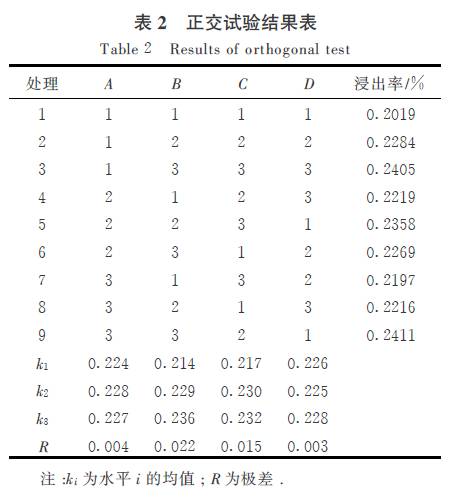
2.3 ���ܹ�����ȡ���ղ�����ȷ�� 2.3.1 ����������ˮƽ����ơ���ѡ��ƾ�Ũ��( A ) ����������ȡ�¶�( B) ������������( C)�ͳ�������ȡʱ��( D)�� ������,���ã� ���أ�ˮƽ����������������� �����ض�ɽ�������ܹ�����ȡЧ����Ӱ��(����) . 2.3.2 �����������������ڵ��������������,���L�� ( ���� ) ��������,���������������� . ���ɱ��� ��֪,������ȡ�¶Ⱥͳ������ʵļ���ֵ�ϴ�,�����ض��ܹ������ȡӰ��Ƚϴ�,���ƾ�Ũ�Ⱥ���ȡʱ�伫��ֵ��Խ�С,���ܹ�����ȡӰ�첻����.�����ض��ܹ�����ȡӰ��Ĵ�С����Ϊ:B ( ��������ȡ�¶�) �� C(��������) �� A ( �ƾ�Ũ��) �� D(��������ȡ ʱ��) .�����ȡ����Ϊ:A�� B�� C�� D�� ,���ƾ�Ũ�ȣ����� ,��ȡ�¶ȣ��� �� ,�����ʣ����� W ,����ʱ�䣳�� min .������������,�ڴ��������ܹ���Ľ�����Ϊ��.���������� .
2.4 ���ܹ�����ʼ����� ����ͨ��HPLC ���ⶨ,����������Ź����������ܹ������Ϊ��.���������� .�ù��յ��ܹ���������Ը�����������,��������ȡ����ȡ�ʣ�.���� mg��g �� �� [ �� ] (����Ϊ��.�������� ) ,��������ȡ����ȡ�ʣ�.���� mg��g �� �� [ �� ] (����Ϊ��.�������� ) ,�Ҵ�������ȡ����ȡ�ʣ�.�� mg��g �� �� [�� ] ( ����Ϊ��.������ ) .�ù���֮�����иߵ��ܹ������,��Ҫ�У� �������ԭ��:һ��ͨ������Ԥ������ĸ��л����ԭ���д����Ƿ�,�������ܹ�����ܳ�;���Ǻ��������µij���������ʹֲ��ϸ�����̶ȵ�����,ʹ�ܹ��������̶ȵĺ���ȡ���Ӵ�,�������ܹ����ܳ�������. �� ���ᡡ�� 3.1 ��ɽ�������ܹ���������ȡ���ռ��ܹ������:���Ͳ���Ϊ�����¶ȣ��� �� ,��ĸ����������ԭ�ϱ�ֵ�� �� ���� ,ҡ��ת�٣����� r ��min�� �� ,ʱ�䣵 d .��������ȡ����Ϊ�ƾ�Ũ�ȣ����� ,��ȡ�¶ȣ��� �� ,�������ʣ����� W ,��ȡʱ�䣳�� min .�ܹ������Ϊ��.���������� . 3.2 ����ĸ���ͷ����������ý�ĸ���ܶ��Ǽ��������オ��,�ں��ʵĹ��ղ�����,�÷�������������ɽ���ǵ��Ƕȶ���Ӱ���ܹ��Ậ��. 3.3 ��������������ȡ���ܹ������ȡ�ʵ���Ҫԭ���dz����������Ŀջ�ЧӦ[�� ] ,����Ч����ϸ����,����ϸ����ͨ��,ǿ������,�Ӷ������ȡЧ��.����������ȡ�ܹ���,�ں��ʵĹ��ղ�������ȡʱ��̡���ȡ�¶Ƚϵ͡����ʸߡ���ݡ��������. 3.4 ���������������ͷ���ȡ�ܹ��Ṥ������������ܹ������,������ȡ�����еĴ����Ѷ�,�����������,Ϊ�ܹ�����ȡ�������˼·,ҲΪɽ�����ۺ����õ춨�˻���. References : [ �� ] ��DAI Jian�\zi , ZHANG Zhi�\hao , TANG Lei , et al . ( ������, ��־��, ����,��) .Progress in research of chemical component and pharmacology of Cornuso f f icinalis [ J] . China Pharmaceuticals ( �й�ҩҵ) ,�������� , ���� : �����\���� . (in Chinese) [ �� ] ��ZHOU Jing�\hua , LI Chun�\sheng , LI Dian�\dong ( �ܾ���,���,��綫) . Progress in research of the activechemical components of Cornus o f f icinalis [ J] .Chinese Journal of New Drugs ( �й���ҩ��־) , �������� ,����(����) : �������\������ . (in Chinese) [ �� ] ��Rajendrasozhan S , Periyaswamy V , Kodukkur V .Protective effect of ursolic acid on ethanol�\mediated experimental liver damage in rats [ J] . Life Sciences ,�������� , ���� : �������\������ . [ �� ] ��XIONG Bin , LEI Zhi�\yong , CHEN Hong ( �ܱ�, ��־��, �º�) . Progress in research of pharmacology of ursolic acid [ J] . Foreign Medical Sciences Section on Pharmacy( ����ҽѧҩѧ�ֲ�) , �������� , ���� ( �� ) : �������\������ . (in Chinese) [ �� ] ����˼�u, ������. ��ĸ���ﻯѧ[ M] . ����: ɽ����ѧ����������, �������� : �����\���� . [ �� ] ��WANG Su�\hui , LI Xia ( ���ջ�, ��ϼ) . Thetechnological conditions of fermentation and reproduction of wine yeast [ J] . Liquor�\Making Science& Technology ( ��ƿƼ�) , �������� , ���� ( �� ) : �����\���� . ( in Chinese) [ �� ] ��ZHAO Yu�\chong , LI Jian�\jun , LIU Guo�\ji , et al .( �����, ���, ������,��) . Extraction of ursolic acid from Cornus o f f icinalis and content determination[ J] . Journal of Zhengzhou University ( ֣�ݴ�ѧѧ��) ,�������� , �� : �����\���� . (in Chinese) [ �� ] ��YANG Zhi�\kun , WANG Shi�\ming ( ��־��, ������) .Extraction of ursolic acid from Cornus O f f icinalis [ J] .Journal of Heilongjiang Cereals and Oils Science and Technology( ���������ͿƼ�) , �������� ( �� ) : �����\���� . ( in Chinese) [ �� ] ��GUO Xiao�\wu (��Т��) . A method of extract chemical components from Chinese herbs with ultrasound [ J] .Natural Product Research and Development( ��Ȼ�����о��뿪��) , �������� , l ( ��) : �����\���� . (in Chinese) ��Ʒ���ӣ� ������ȡ�� ��ԭ�� ��������ȡ�� �������� ����Ҷ��ȡ��-�ܹ��� ����ޱ��ȡ��-�������� �Ϻ����� רעֲ�� ���ڸߴ� ����������Ȼ��������������� |







 ��������������ȡɽ���Ƿ��Ͳ����е��ܹ���
��������������ȡɽ���Ƿ��Ͳ����е��ܹ���