-
邢国秀1 , 李 楠1 , 杨美燕1 , 崔丽钧1 , 王 童2
-
(1. 大连理工大学化工学院,辽宁大连116012 ;2. 辽宁中医学院,辽宁沈阳110032)
- 关键词:苦杏仁苷;综述;药理作用;分析
-
- 苦杏仁苷是传统中药苦杏仁中的有效成分,人们对它的研究已有近二百年的历史,早在1803 年Schrader 在研究苦杏仁成分时就发现了此类物质,直到1830 年Robiquet 等从中分离出苦杏仁苷,迄今它已成为医药上常用的祛痰止咳剂、辅助性抗癌药物,苦杏仁苷广泛存在于杏、桃、李子、苹果、山楂等多种蔷薇科植物果实的种子中,尤其在苦杏仁中含量较多,大约在2 %~3 %。苦杏仁苷分子由一单元苯甲醛、一单元氢氰酸和两单元葡萄糖组成。其分子式为C20 H27NO11 ,结构式为:
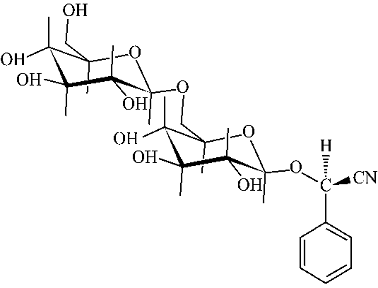
- 1 苦杏仁苷的药理学研究进展
- 1. 1 镇咳平喘作用 苦杏仁苷内服后,可在体内分解为氢氰酸和苯甲醛,氢氰酸对呼吸中枢可产生一定的抑制作用,使呼吸运动趋于安静而达到镇咳平喘的作用[ 1 ] 。苦杏仁苷对油酸型呼吸窘迫症动物可促进肺表面活性物质的合成,并使病变得到改善。
-
- 1. 2 抗肿瘤作用 苦杏仁苷具有良好的抗肿瘤作用,被用作治疗癌症的辅助药物。将苦杏仁苷制剂用于晚期癌症患者的治疗,可使症状改善,存活期延长。将苦杏仁苷用于癌性胸水的治疗,发现苦杏仁苷对癌性胸水有一定程度的控制和缓解作用。将苦杏仁苷按300mg・kg - 1 , 400mg・kg - 1 ,600mg・kg - 1剂量给移植性肝癌小鼠腹腔注射10~14d ,其肝癌治愈率分别为72 % ,60. 8 % ,61 %。移植性肝癌小鼠肝脏微粒体细胞色素P2450 含量比正常小鼠显著下降。当苦杏仁苷给药10d ,肿瘤生长被抑制的小鼠P2450 含量达到正常水平[ 2 ] 。苦杏仁苷对子宫颈癌JJC26 株的抑制率为50 %~70 %。苦杏仁苷及其水解所产生的氢氰酸和苯甲醛体外试验均被证明有抗癌作用,癌细胞内硫氢化酶较正常细胞少,因此对苦杏仁苷水解释放出氢氰酸的解毒能力较差,苦杏仁苷加苯甲醛或苦杏仁苷加β2葡糖苷酶可明显提高抗癌效力,已发现癌细胞无氧酵解占优势,其产物乳酸形成的偏酸性环境有利于提高β2葡糖苷酶的活性,促使苦杏仁苷在癌细胞中水解出较多的氢氰酸和苯甲醛而发挥更强的抗癌作用。
-
- 1. 3 对消化系统的影响 苦杏仁苷在经酶作用分解形成氢氰酸的同时,也产生苯甲醛,后者可抑制胃蛋白酶的活性,从而影响消化功能。杏仁水溶性部分的胃蛋白酶水解产物500mg・kg - 1的剂量对四氯化碳处理的大鼠给药,发现它能抑制AST、AL T 水平和羟脯氨酸含量的升高,并抑制优球蛋白溶解时间的延长。在病理学上,杏仁水溶部分的胃蛋白酶水解产物能抑制鼠肝结缔组织的增生,但不能抑制D2半乳糖氨引起的鼠AST、AL T 水平升高。
-
- 1. 4 其他作用 苦杏仁苷可特异性地抑制阿脲所致血糖升高,作用强度与血液中苦杏仁苷浓度有关。苦杏仁苷还具有抗凝血作用。小鼠热板法和醋酸扭体法证实苦杏仁苷有镇痛作用且无耐受性;小鼠给予苦杏仁苷后无竖尾反应和烯丙吗啡诱发的跳跃反应[ 3 ] 。苦杏仁苷15mg・只- 1 ,35mg・只- 1给小鼠肌注,可明显促进有丝分裂原对小鼠脾脏T 淋巴细胞的增殖。将大鼠鼠脑右额颞叶快速冰冻切片进行细胞色素氧化酶孵育染色,染色系统通过显微电视图像测量系统观察,数据经微机处理,结果表明苦杏仁苷有明显提高脑缺血状态下细胞色素氧化酶活性的作用[ 4 ] 。苦杏仁苷在最佳浓度范围和作用时间内能提高人肾成纤维细胞( KFB) 分泌的I型胶原酶活性的作用,抑制人肾KFB 增值和I 型胶原的表达,促使人肾KFB 凋亡[ 5 ] 。苦杏仁苷与冬虫夏草联合作用与体外原代单层培养得大鼠纤维肝肝细胞,用EL ISA 方法监测表明苦杏仁苷与冬虫夏草具有明显提高大鼠纤维肝肝细胞合成分泌白蛋白的作用[ 6 ] 。以99Mtc2植酸钠注入小鼠或肝组织印片Ag2NOR 法观察苦杏仁苷对小鼠肝细胞吞噬功能或rDNA 活化作用的影响,结果表明苦杏仁苷对其吞噬功能及rDNA 的活化均有非常明显的促进作用。
-
- 1. 5 毒性 苦杏仁苷的急性毒性试验LD50小鼠静脉注射为25g・kg - 1 ;大鼠静脉注射为25g・kg - 1 ,腹腔注射为8g・kg - 1 。最大耐受量:小鼠兔犬静注和肌注均为3g・kg - 1 ,口服均为0. 075g・kg - 1 。人静脉注射为5g(约0. 07g・kg - 1) [ 7 ] 。小鼠按500mg・kg - 1静注10 只,均未死亡,而以同样剂量灌胃给药,则10 只死亡8 只。口服给药的毒性所以大于静脉给药,研究证明主要是由于苦杏仁苷被肠道微生物水解产生较多的氢氰酸所致,如果处理小鼠使其肠道内微生物抑制,则胃肠给药300mg・kg - 1未出现死亡现象,如未经处理,则相
- 同剂量死亡率为60 %。人口服B17 (苦杏仁苷) 每日4g ,持续半个月或静脉注射一个月可见毒性反应,以消化系统较为多见,此外还表现为心电图T 波改变、房性早博,停药后以上毒性反应均可消失。如果剂量减为每日口服0. 6~1g ,则可避免毒性。
-
- 2 苦杏仁苷分析方法进展
- 2. 1 间接法 间接法的原理是通过水解或酶解把苦杏仁苷分解为苯甲醛、氢氰酸和葡萄糖,然后再测定相应分解物的含量来间接分析苦杏仁苷。间接法包括中国药典法[ 8 ] 、化学
- 发光法、电化学分析法等。
-
- 2. 1. 1 中国药典法(即银量法) :使苦杏仁苷酶解产生氢氰酸,通水蒸气蒸馏,溜出液导入氨试液中,用硝酸银滴定液滴定吸收了氢氰酸的氨试液,从而测定苦杏仁苷的分析方法。
-
- 2. 1. 2 化学发光法:化学发光是一种具有极高灵敏度和良好选择性的微量及痕量分析技术。宋正华、章竹君把流动注射分析技术和化学发光法结合起来,设计了苦杏仁苷化学发
- 光传感器,这种新型生物传感器的化学发光强度与苦杏仁苷量在1~200μg 之间成良好线性关系,具有良好选择性[ 9 ] 。
-
- 2. 1. 3 电化学分析方法:是使用一种或多种对苦杏仁苷具有水解活性的酶处理被分析物,从而产生氰根离子再用电极测定氰根离子浓度分析苦杏仁苷的方法。由于这种方法在测量微量痕量苦杏仁苷具有明显的优势,而且易于分析测定工作自动化,近些年来发展迅速,出现了多种苦杏仁苷生物传感器: Tatsuma 等发展了一种基于干扰信号检测的苦杏仁苷生物传感器,这种传感器将辣根过氧酶(HRP) 和β2葡糖苷酶固定在热解石墨上,通过测定由于积累过氧化氢造成的氰根阴极电流的抑制作用来测定苦杏仁苷的含量[ 10 ] 。Merko2ci ,A 设计了把β2葡糖苷酶同银盐混合物固定于生物膜上的生物传感器[ 11 ] 。上述传感器在各自相应的测量范围内具有良好的线性关系。
-
- 2. 2 直接法
-
- 2. 2. 1 薄层扫描法:薄层扫描法是一种简捷快速的分析方法,灵敏度较高,可直接测定植物种子中的苦杏仁苷含量。
-
- 2. 2. 2 高效液相色谱法 高效液相色谱法分离效率高,分析速度快,现已成为有机物定性定量分析研究的主要方法。Kimerly Wasserkrug ,Ziad Elpassi 用硅柱反相高效液相色谱仪检测并分离了苦杏仁苷,并比较了用脉冲电流检测器与紫外吸收检测器检测之间的不同[ 12 ] 。Seong ho kang 等用高效液相色谱和质谱鉴定了苦杏仁苷和它的异构体[ 13 ] 。
-
- 2. 2. 3 紫外分光光度法 分光光度法是分析化学中普遍应用的一种方法,这种方法具有快速灵敏准确的特点,所用仪器结构简单,造价低廉,使用方便,适宜作为常规分析的工具。
-
- 2. 2. 4 毛细管胶束电泳色谱 毛细管电泳色谱是近年来发展最快的分析分离方法,它是经典电泳技术和现代微柱分离相结合的产物,具有高灵敏度、高分辨率、高速度、样品用量少、成本低等优点。由于苦杏仁苷是水溶性物质,用毛细管胶束电泳色谱[MEKC]分离苦杏仁苷效果极佳。Seong Ho Kang 等采用毛细管胶束电泳色谱成功地分析了苦杏仁苷和它的异构体,并用高效液相色谱、紫外分光光度计和质谱进行验证,结果一致。C. Campa 等用毛细管胶束电泳色谱研究了不同pH 值、不同时间苦杏仁苷的水解情况[ 14 ] 。Isozak2i ,Takafumi 等用环糊精修饰的毛细管胶束电泳色谱分离测定了苦杏仁苷及其异构体[ 15 ] 。
-
- 2. 2. 5 色谱2质谱联用技术 色谱法作为一种大有所为的近代分离技术普遍应用于有机化合物的分离分析中,质谱仪灵敏度高,特征性强,要求分析样品必须是高度纯净物。色谱技术为质谱分析提供色谱纯的式样,质谱为色谱仪提供准确的结构信息,彼此之间的依赖性促成了色谱/ 质谱的联用。David Chassage 等用气相色谱/ 电子轰击质谱[ GC/ EI2MS]和气相色谱/ 负离子化学离解质谱[ GC/ NCI2MS]联用从多种水果中分离分析了苦杏仁苷[ 16 ] 。
-
- 3 苦杏仁苷分离提取研究进展
- 提取苦杏仁苷可采用80 %乙醇或加水煮沸数分钟,残渣加水用石油醚或氯仿提取除去脂溶性成分,亦可用乙酸乙脂等溶剂进行液液分配萃取或用甲醇与乙酸乙酯恒沸混合溶剂提取,这样可避免大量极性化合物如糖、氨基酸、肽类成分溶出;或将所得水液先用醋酸铅、聚酰胺或混合型离子树脂等进行预处理,除去其中酸性、酚性及离子性化合物,经处理后的水液减压浓缩,再用柱层析进行分离纯化,其填料一般是硅胶、硅藻土、硅酸镁、活性炭、纤维素或彼此联合使用。由于苦杏仁苷在冷乙醇中的溶解度很小,在热乙醇中的溶解度很大,所以亦可采用乙醇做结晶溶剂提取苦杏仁苷,原料经过预处理和压榨,用95 %的乙醇浸提两次后进行脱脂处理,得到脱脂粕,脱脂粕经过粉碎后,用沸醇回流装置进行萃取,经结晶、重结晶和纯化,便可得到苦杏仁苷[ 17 ] 。苏碧茹等用正交实验法进行了苦杏仁成分提取工艺的优选研究,他们选取溶媒浓度、溶媒量、提取时间、提取次数为试验因素,得出最佳工艺条件为95 %乙醇提取两次,每次1h ,6 倍量乙醇为最佳工艺,由此工艺制得苦杏仁霜[ 18 ] 。
-
- 4 小结
- 综上所述,苦杏仁苷具有明确的生理、药理活性。在苦杏仁苷的分析研究方面,人们已作了大量的工作,苦杏仁苷的分析检测方法比较完善,但国内对苦杏仁苷分离提取工艺的深入研究较少,所以对苦杏仁苷提取工艺进行系统的研究并进行药品开发具有重要应用价值。
-
-
- 参考文献:
- [ 1 ] 周金黄,王筠默. 中药药理学[M] . 上海:上海科学技术出版社,1986 :219.
- [ 2 ] 车文一,金泰日,张良和,等. 苦杏仁提取物的抗癌作用及其对移植性肝癌小鼠细胞色素P2450 含量和谷胱苷肽S2转移酶活性的影响[J ] . 延边医学院学报,1987 ,10 (4) :223.
- [ 3 ] 朱友平,苏中武,李承祜. 苦杏仁苷的镇痛作用和无身体依赖性[J ] . 中国中药杂志,1994 ,19 (2) :105.
- [ 4 ] 杨俊何,黄勤,杨小平,等. 苦杏仁苷对脑缺血能量代谢中细胞色素氧化酶的影响[J ] . 中药新药及临床药理,1996 ,7 (2) :50251.
- [ 5 ] 屈燧林. 汉防己甲素、川芎嗪和苦杏仁苷对人肾成纤维的影响[J ] . 中华肾脏病杂志,2000 ,16 (3) :1862189.
- [ 6 ] 李旭东,王树槐,蒋家道. 扶正化瘀中药体外对大鼠纤维肝肝细胞蛋白合成、分泌的影响[J ] . 中成药,2001 ,23 ( 4) : 2742277.
- [ 7 ] 郭晓庄. 有毒中草药大辞典[M] . 天津:科技翻译出版公司,1992 :292.
- [ 8 ] 中华人民共和国药典[ S] . 一部,160 ,2000.
- [ 9 ] 宋正华,章竹君. 苦杏仁苷化学发光生物传感器[J ] . 分析化学,2000 ,28 (8) :9642967.
- [ 10 ] Tetsu T , Koichiro T , et al. Interference - based amydalin sensor with emulsin and peroxidase [ J ] . Senors and Actuators B49(1998) :268.
- [11 ] Merkoci A , Braga S. A potentiometric biosensor for D2amyg2 dalin based on a consolidated biocomposite membrane [J ] . Ana2 lytica Chimica Acta , 391 (1999) :65272.
- [ 12 ] Kimberly W K, Ziad EI R. High performance liquid phase sepa2 ration of glycosides. i. reversed phase chromatography of cyanogenic glycosides with UV and pulsed amperometric detec2 tion[ J ] . Journal of Liquid Chromatography & Related Tech2 nologies , 1997 , 20 (3) :3352349.
- [ 13 ] Seong H K, Hyunsook J , et al. Miceller eletrokinetic chromato2 graphy for the analysis of D2amygdalin and its epimer in apricot[J ] . Journal of Chromatography A , 866 (2000) :2532259.
- [ 14 ] Campa C. , Schmitt2Kopplin PH. , et al. Analysis of cyanogenic glycosides by micellar capillaryelectrophoresis [ J ] . Journal of Chromatography B , 739 (2000) :952100.
- [15 ] Isozaki , T F , et al. Quantitative determination of amydalin epimers by cyclodextrin2modified micellar electrokinetic chro2 matography[J ] . J of Chrom. A , 923 (2001) :2492254.
- [16 ] David C , Jean C C , et al. Identification and quantification of passion fruit cyanogenic glycosides. J Agric Food Chem. 1996 ,44 :381723820.
- [ 17 ] 车凤斌. 苦杏仁苷提取工艺研究[J ] . 食品工业科技,1997 ,3 :11213.
- [18 ] 苏碧茹,黄小虹. 正交试验法优选苦杏仁成分的提取工艺[J ] . 中药材,1999 ,22 (2) :93294.
相关产品链接:
苦杏仁苷 枇杷叶提取物-熊果酸 杜仲提取物 绿原酸 金银花提取物 大花紫薇提取物-科罗索酸
淫羊藿苷
上禾生物,专注植提,精于高纯
基于您对天然产物需求持续创新
-
|
 天然苦杏仁苷的研究进展 NEWS
天然苦杏仁苷的研究进展 NEWS